Tipp: Blanke Glücks-Cent verschenken – Kupfermünzen reinigen
Nein, ihr seid nicht im falschen Blog. 🙂 Es geht bei mir immer noch rund um Natur und Wissenschaft. Deshalb gibt es hier nicht nur einen Reinigungstipp, sondern wir schauen uns auch an, was bei der Münzreinigung passiert.
Vielleicht habt ihr schon mitbekommen, dass ich auch gerne bastele. Dazu gehört für mich auch das hübsche Verpacken von Geschenken. Um – je nach Anlass – auch ein wenig Glück zu wünschen, kommt ein „Glücks-Cent“ wie gerufen. Gerade jetzt zum Jahreswechsel stehen gute Wünsche für das Neue Jahr hoch im Kurs. Leider sind die Kupfermünzen oft schwarz angelaufen und nicht mehr blank.
Wie werden Kupfermünzen wieder blank?
Schwarze Kupfermünzen können am preiswertesten mit einfachem Haushaltsessig gereinigt werden. Ihr gießt den Essig in ein Glas und gebt etwas Salz hinzu. Das Salz sorgt dafür, dass die Münze schneller kupfern glänzt. Sobald die Münze blank ist, wird sie aus der Essiglösung genommen, mit Wasser abgespült und getrocknet.
Diese schnelle Reinigungsmethode eignet sich gut für eine Centmünze, aber sie sollte auf keinen Fall für wertvolle Münzen verwendet werden. Weshalb das so ist, schauen wir uns gleich an.
Warum werden Kupfermünzen schwarz?
Kupfermünzen werden schwarz, weil sie mit dem Sauerstoff aus der Luft zu schwarzem Kupferoxid (genauer: Kupfer(II)-oxid) reagieren. Hier unsere Reaktionsgleichung: (Ich habe die Gleichung auch direkt in der Symbolsprache dazu geschrieben. So ist die Reaktionsgleichung international.)
Kupfer + Sauerstoff → Kupferoxid
2 Cu + O2 →2 CuO
(Der Pfeil bedeutet „reagiert zu“.)
Natürlich könnte man versuchen diese Schicht mechanisch mit Reiben zu entfernen. Die Oberfläche ist allerdings glatter und glänzt mehr, wenn Kupferoxid in einer verdünnten Säure, wie beispielsweise in Haushaltsessig, gelöst wird. „Verdünnt“ bedeutet, dass neben der eigentlichen Säure noch jede Menge Wasser vorhanden ist. Mein Essig enthält zum Beispiel 5% Säure. Dann schauen wir uns mal „die Chemie“ der Kupferreinigung an. 😉
Kupferoxid + Essigsäure → Wasser + Kupferacetat (gelöst)
CuO + 2 CH3-COOH → (CH3-COO)2Cu + H2O
In der Chemie geht nichts verloren. 😉 Das zeigt die Reaktionsgleichung in Symbolschreibweise. Auf jeder Seite des Pfeils finden wir die gleich viel Kupfer (Cu), Sauerstoff (O), Wasserstoff (H) und Kohlenstoff (C). Wir nennen das „Das Gesetz zur Erhaltung der Masse“. Das bedeutet, dass alles was auf der linken Seite des Pfeils zu finden ist, auch auf der rechten Seite auftauchen muss. Der Sauerstoff aus dem Kupferoxid reagiert mit dem Wasserstoff aus der Essigsäure zu Wasser. Übrig bleiben positiv geladene Kupferionen und negativ geladene Essigsäureionen, die sich gut im wässrigen Haushaltsessig lösen.
Ionen? Was ist denn das schon wieder?
Mit Ionen werden positiv oder negativ geladene Teilchen bezeichnet, wie ich es oben beschrieben habe. Wenn hingegen der Begriff „Atom“ verwendet wird, sind immer ungeladene Teilchen gemeint.
Unsichtbare Kupferionen sichtbar machen
Kupfer(II)-acetat ist auch als Grünspan bekannt. Allerdings ist die Menge bei unserer Reaktion so gering, das keine Farbveränderung sichtbar ist. Das Metall Kupfer lässt sich jedoch gut anhand der rötlichen Farbe nachweisen. Gut – eine einzelne Münze reicht für diesen Nachweis nicht. Je nachdem wie dunkel die Münzen sind, also der Menge Kupferoxid, werden etwa 20 bis 30 Kupfermünzen gebraucht. Ein paar mehr schaden nicht, dann sieht man das Ergebnis schneller. 😉
Wir brauchen wieder Haushaltsessig, Kochsalz, Kupfermünzen und diesmal zusätzlich einen Eisennagel. Der Nagel sollte blank und nicht verrostet sein. Das Salz im Essig lösen und die Münzen sowie den Nagel in die Lösung legen. Nun heißt es ungefähr eine halbe Stunde warten. Dann wieder die Münzen und den Nagel in Wasser reinigen. Der Nagel hat jetzt einen kupferfarbenen Überzug. Da es keine „dicke“ Kupferschicht ist, hatte ich leider ein paar Schwierigkeiten mit dem Fotografieren und den aktuellen Lichtverhältnissen. 😦
Was ist passiert?
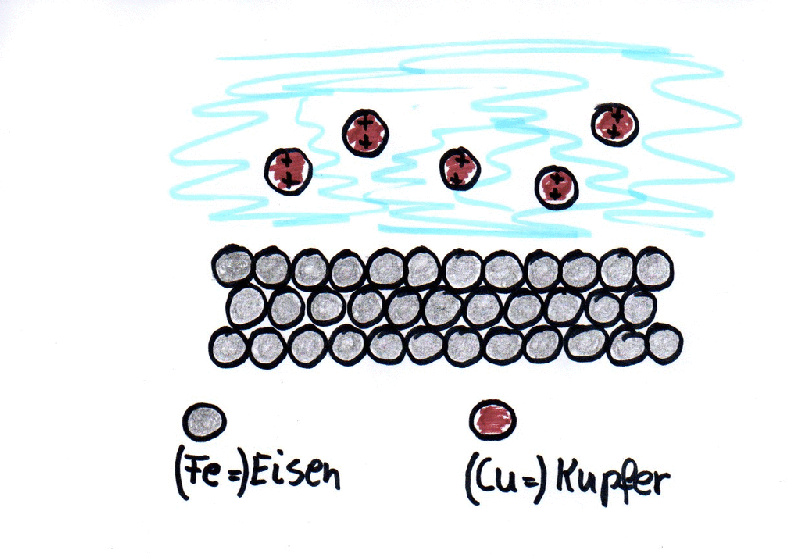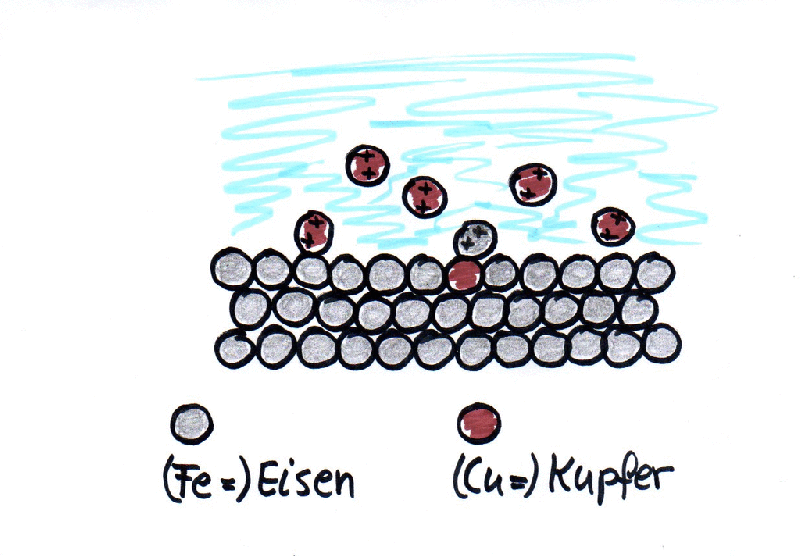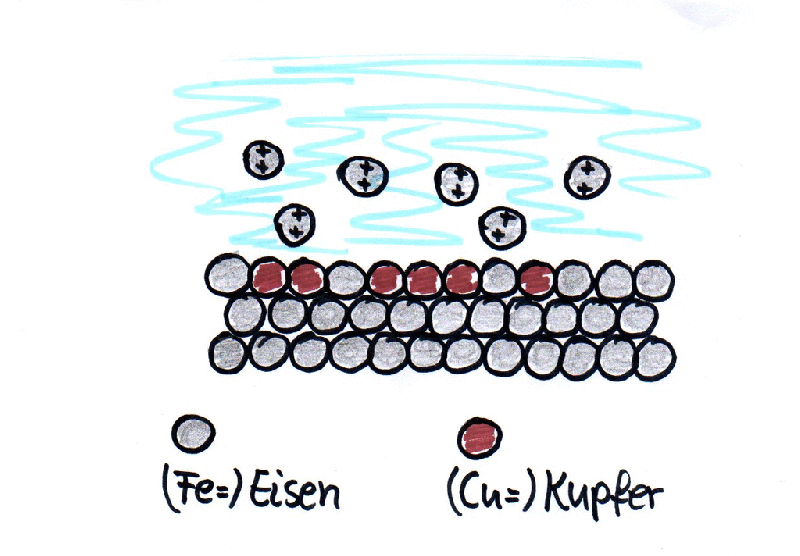
Da Eisen unedler ist als Kupfer haben die Eisenatome und die Kupferionen ihren Platz getauscht:
Eisenatome + Kupferionen → Kupferatome + Eisenionen
Fe + Cu2+ → Cu + Fe2+
Und mit dem Kupfer auf dem Eisennagel wird auch deutlich sichtbar, weshalb sich diese Reinigungsmethode nicht für wertvolle Münzen eignet: Die Münzen werden weniger, da das Kupfer in die Lösung übergeht.
Zum Schluss noch ein Tipp: Im Beitrag „Eis mit Eis kühlen“ findet ihr auch haushaltstaugliche Chemie. 😉
Veröffentlicht am Dezember 13, 2019 in NATUR + WISSENSCHAFT und mit Eisen, Essig, Glücksbringer, Kupfer reinigen, Kupfermünze, Kupferoxid getaggt. Setze ein Lesezeichen auf den Permalink. Ein Kommentar.

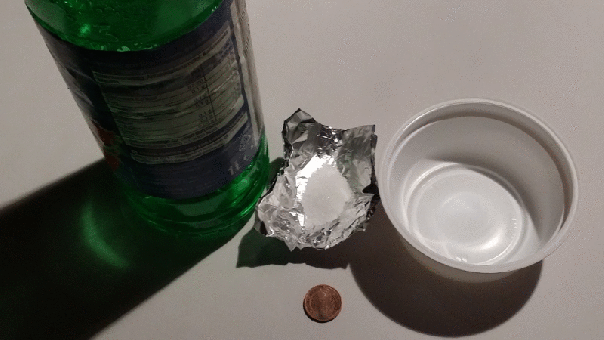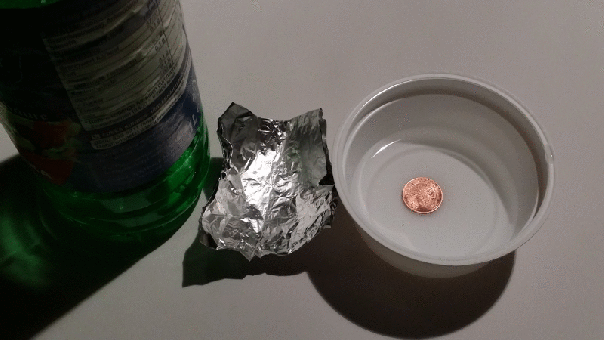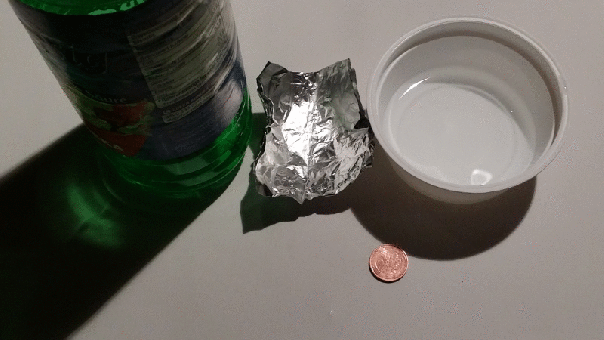
Pingback: Klimawandel und Mobilität oder besser: Mobil mit Klimaschutz | Natur-Wissenschaft-Blog